شوک: نارسایی متابولیکی سلولی در بیماری وخیم
شوک: نارسایی متابولیکی سلولی در بیماری وخیم
شوک: نارسایی متابولیکی سلولی در بیماری وخیم
تنظیم: دکتر حسین موسوی، دکتر شیما نبائی، دکتر کیوان اسدی
فرمت: PDF تعداد صفحات: 26
فهرست:
- فیزیولوژی طبیعی گردش خون و التهاب (فیزیولوژی بطنی، بازگشت وریدی، فیزیولوژی التهاب)
- شرایط کمبود خونرسانی (هیپوپرفیوژن) (پاسخ عصبی خونی به هیپوپرفیوژن، تاثیر هیپوپرفیوژن بر التهاب و متابولیسم سلولی)
- سبب شناسی، تشخیص و مدیریت شرایط هیپوپرفیوژن (درمان هیپوولمی، کاهش بازگشت خون وریدی: تامپوناد پریکاردیال، نقطه پایان احیاء گردش خون)
- شرایط التهابی شدید (تاثیر التهاب شدید بر گردش خون و عملکرد سلولی)
- راهنمای بالینی به بیماری که در شوک است
- نمونه سوالات تستی + پاسخ تشریحی
اهداف
- توصیف شوک و توضیح دو مکانیسم اولیه ای که منجر به اختلال عملکرد سلول ها در هنگام شوک می شود.
- توضیح علل این مکانیسم های اولیه که منجر به ایجاد شوک می شود.
- توضیح اطلاعات بالینی (به طور مثال، سابقه بیماری، معاینه فیزیکی، تست های تشخیصی و شاخص های همودینامیکی) که در تعیین آنکه کدام یک از دو مکانیسم اولیه، علت غالب ایجاد شوک در یک شخص است کمک می کند.
- توضیح رابطه متقابل بین دو علت اولیه شوک در تخریب سلولی
- توضیح اصول اولیه درمانی که منجر به کاهش آسیب ناشی از مکانیسم های اولیه شوک می شود
غالبا تعریف قدیمی شوک، از فشار خون سیستولیک کمتر از ۹۰mmHg به عنوان یک معیار استفاده می شد. بر طبق این معیار، رده بندی شوک به هیپوولمیک / هموراژیک، سپتیک، کاردیوژنیک و شوک نوروژنیک که طبقه بندی می شوند و نشان می دهد که دلیل تغییر گردش خون در تشخیص گذاشتن مهم است. گرچه، اتیولوژی مشخص هیپوتانسیون (مثل گشادی عروق عصبی بعد از صدمه طناب نخاعی) الزاما باعث صدمه سلولی یا اندام نمی شود. علاوه بر این، صدمه اندام یا سلولی ممکن است بدون رسیدن هیپوتانسیون به mmHg ۹۰ پیشرفت کند. بنابراین، تعریف شوک بر اساس اندازه گیری فشار خون سیستولی به طور بالقوه باعث اشتباه و وسعت کم می شود.
تعریف وسیع تر این است که شوک شرایطی است که متابولیسم سلولی کل بدن بد عمل می کند. این مفهوم به تاریخ ۱۸۷۲ برمی گردد وقتی که آقای گروس شوک را به عنوان یک مختل کننده زندگی توصیف می کرد. وقتی که تهدید به طور تهاجمی است، متابولیسم سلولی کار نمی کند ولی برگشت پذیر است. ولی در صورتی که ادامه پیدا کند شوک منجر به فرایند مرگ سلولی، صدمه اندام و مرگ احتمالی فردی می شود. در طول قرن ۲۰ خیلی از تئوری هایی در توضیح به این صدمه سلولی و مرگ (مثل اختلال گردش خون، اختلال سیستم عصبی، مسمومیت) گسترش پیدا کرد.
در سال ۱۹۵۰، دو تئوری برجسته در رقابت بودند. ۱) شوک به طور ثانویه، تحویل اکسیژن به مقدار ناکافی است. ۲) شوک به طور ثانویه نتیجه سمیت سلولی است که می تواند پیشرفت کند حتی وقتی که اکسیژن کافی تحویل داده شده است. این شرایط به عنوان خونریزی شدید و بد عمل کردن قلب (مثل خون رسانی کم) در طول یک قرن به عنوان اتیولوژی تحویل ناکافی اکسیژن شناخته شده بود. شناخت این که مواد سمی اولیه در صدمه سلولی مواد اندوژن ناشی از پاسخ التهابی سلول آسیب دیده هستند نه سموم اگزوژن در طول ۳ دهه گذشته پدیدار شد. صدمه بافتی و نتیجه پاسخ التهابی مرتبط با آن در تولید یا فعالیت مولکولی (مثل سیتوکین ها، رادیکال های آزاد، پروستاگلاندین ها، چسبندگی مولکولی) فعالیت سلولی محیطی را بیشتر می کند، بافت را ترمیم می کند و از سلول میزبان دفاع می کند.
گرچه، بعضی اوقات این پاسخ محیطی پاسخ های مشابه ای را در سایر سلول ها تحریک می کند که از محل اولیه دور هستند. و در نتیجه این سیستم التهابی است که نقص عملکرد سلولی و شوک ایجاد می شود. به صورت همزمان، در طول ۲ دهه گذشته مطالعات کلینیکی و آزمایشهایی نشان داد که این ۲ مکانیسم صدمه سلولی به صورت رقابتی یا انحصاری نیستند بلکه در طول حالت شوک اغلب بیشتر موارد افزایشی با هم عمل می کنند. “در حالت ساده، خون رسانی کم سبب التهاب و التهاب سبب خون رسانی کم می شود.” پزشکان می بایست به این همراهی آگاه باشند و می بایست هر بیماری را که علائم بد عملکردی سلولی کل بدن را دارد با ۲ هدف ارزیابی دقیق گردش خون برای تحویل اکسیژن و حالت التهابی برای سمیت سلولی رسیدگی کنند. ترميم گردش خون و بهبود التهاب شدید از اصول اولیه برای مدیریت کردن بیمار شوک دار هستند.
این بخش پاتوفیزیولوژی را توضیح می دهد که پرفیوژن بافتی کم با التهاب مرتبط هستند و راهنمایی هایی کلینیکی برای تشخیص خون رسانی کم و التهاب شدید ارائه میدهد و استراتژی های مدیریتی که می تواند این مکانیسم های سلولی را محدود کند، طرح می کند.
فیزیولوژی طبیعی گردش خون و التهاب
عملکرد اصلی گردش خون تحویل اکسیژن به مویرگ ها است. تعیین کننده های تحویل اکسیژن به کل بدن در ارتباط با سایر متغیرهای یا همودینامیکی در جدول ۱ لیست شده است. به عنوان یک قاعده برای تحویل اکسیژن نشان میدهد که جز ریوی در عرضه کافی اشباع اکسیژن شریانی محدودیت دارد (اشباع و عرضه بیشتر از ۹۰٪ اکسیژن وقتی که فشار اکسیژن بیشتر از mmHg ۶۰ باشد). وقتی این هدف معمولا به آسانی با درمان تنفسی مدرن به انجام می رسد. هموگلوبین می تواند با تزریق گلبول قرمز افزایش یابد اما این استراتژی در اجرا محدودیت دارد. معمولا، سخت ترین جز درمان خروجی قلبی است. تعیین کننده خروجی قلبی به وسیله متغیرهایی که بر عملکرد بطنی تأثیر می گذارد و متغیرهایی که بر بازگشت وریدی تاثیر می گذارد سازماندهی می شود. بر اساس موقعیت های کلینیکی، گاهی اوقات تغییرات در فیزیولوژی بطنی تا گردش خون بهتر شود مفید است و گاهی اوقات تغییرات در فیزیولوژی بازگشت وریدی مفید است.
TABLE 1: Hemodynamic and Oxygen Delivery Variables
|
Normal |
Definition | Item |
| 5-15 mm Hg | Central venous pressure; CVP = RAP in the absence of tricuspid valve disease. CVP = RVEDP |
CVP |
|
5-15 mm Hg |
Left atrial pressure; in the absence of mitral valve disease, LAP – LVEDP | LAP |
| 5-15 mm Hg | Pulmonary capillary occlusion pressure, PAOP = LAP, except sometimes with high PEEP levels |
PAOP |
|
80-90 mm Hg |
Mean arterial pressure, mm Hg: MAP = OP + 1/3 (SP-DP) | MAP |
| 2.5-3.5 L/min/m2 BSA | Cardiac index: CI-CO/m2 BSA |
Cl |
|
35-40 mL/beat/m2 |
Stroke index: SI = SV/m2 BSA | SI |
| 1000-1500 dyne-s/cm5 | Systemic vascular resistance: SVR = (MAP-CVP) × 80/C0 |
SVR |
|
100-400 dyne-s/cm5 |
Pulmonary vascular resistance: PVR = (MAP – PAOP) × 80/CO | PVR |
| 20 vol % | Arterial oxygen content (vol%); CaO2 =1.39 × Hgb SVO2 + (PaO2 × 0.0031) |
CaO2 |
|
15vol% |
Mixed venous oxygen content (vol%); CVO2 = 1.39 x Hgb × SVO2 + (PVO2 × 0.0031) | CVO2V |
| 3.5-4.5 vol% | Arterial venous O2 content difference; C(a-v)O2 = CaO2 – CVO2 (vol%) |
C(a-v)O2 |
|
900-1200 mL/min |
O2 delivery: O2D = CO x CaO2 x 10; 10 = factor to convert mL O2/100 ml blood to ml O2/L blood | O2D |
| 250 mL/min | O2 consumption; O2C = (CaO2 – CVO2) CO x 10 |
O2C |
|
BSA body surface area (m2): Co. cardiac output: Op diastolic pressure, ZVEDP left ventricular and diastolic pressure: PaO2, PAOP pulmonary artery occlusion pressure PEEP. positive end-expiratory pressure, arterial PO2 mmHg: PVO2 mixed venous PO2 RAP right atrial pressure, RVED. right ventricular and diastolic pressure Sao2 arterial per saturation (%) SVO2 mixed venous oxygen Saturation SP systolic pressure, Stroke volume. |
||
این تقاضای منطقی یک فیزیولوژی گردش خون در برابر دیگری (فیزیولوژیک در جزییات بیشتر در قسمت خونرسانی کم) توضیح میدهد.
فیزیولوژی بطنی تعیین کننده های اصلی کارایی بطنی در جدول ۲ لیست می شود. پره لود حجم کشش میوکاردی است، محرک انقباض ماهیچه ای به وسیله مکانیسم فرانک استارلینگ توضیح داده میشود که از آن طریق افزایش کشش به افزایش انقباض منتهی می شود تا اینکه عضله بیش از حد کشش یابد (به طور معمول تشخیص کلینیکی نارسایی مزمن قلبي داده می شود).
پره لود اختصاصی ترین سنجه به عنوان حجم پایان دیاستولی است. زیرا حجم به آسانی از نظر بالینی قابل اندازه گیری نمی باشد، نسبت مستقیم بین حجم بطنی و فشار پایان دیاستولی بطنی به اندازه گیری فشار (معمولا سنجش فشار ورید مرکزی برای قسمت راست قلب و گوه مویرگی ریوی یا فشار انسدادی شریان ریوی برای سمت چپ قلب برای تخمین حجم اجازه می دهد. افترلود بطنی اصولا به وسیله مقاومت برای خروج بطنی که هم توسط ریه مقاومت عروق ریوی) یا درخت سیستمیک شریانی (مقاومت عروقی سیستمیک) تعیین می شود.
با پره لود پایدار، افزایش افترلود خروج بطنی را کم می کند و کاهش افتر لود خروجی را زیاد می کند. تحریک پذیری نیروی انقباضی تحت شرایط از پیش تعیین شده پره لود و افترلود است. فاکتورهایی که ممکن است باعث افزایش یا کاهش تحریک پذیری شود در جدول ۳ لیست شده است. تغییر در تحریک پذیری، مثل تغییر در افتر لود، نتیجه هایی متفاوت در منحنی عملکرد قلب دارد. ترکیب تأثیر افزایش تحریک پذیری و کاهش افترلود در بهتر کردن عملکرد بطنی در شکل ۱ نشان داده شده است. ضربان قلب با خروجی قلب نسبت مستقیم دارد (نه با مکانیسم های عضله قلب) تا اینکه ضربان سریع پر شدن بطنی در طول دیاستول را کم کند.
TABLE 2: Determinants of Ventricular Function
|
Preload |
|
Afterload |
|
Contractility |
|
Heart rate |
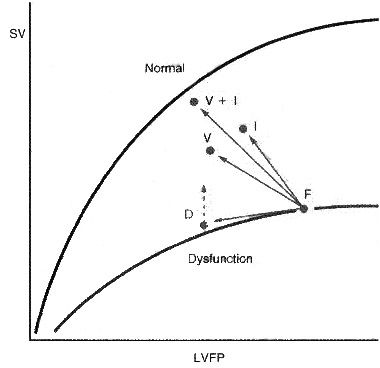
FIGURE 1. Expected hemodynamic response in severe left ventricular dysfunction to administration of diuretics (D), inotropic drugs (). vasodilators (V), and a combination of vasodilators and inotropics (V+). SV, stroke volume; LVFP, left ventricular filling pressure; F, failure.
بازگشت وریدی
بازگشت وریدی با این فرمول توضیح داده می شود
VR= (MSP-CVP) (RV+ RA/19)
MSP: میانگین فشار سیستمیک CVP، فشار ورید مرکزی (فشار شریان راست) RV: مقاومت وریدی و RA مقاومت شریانی باشد. این معادله به وسیله گایتون در سال ۱۹۷۳ هم با محاسبه و با مشاهده تجربی به صورت فرمول در آمد. از احتمالات مورد انتظار، تغییرات در مقاومت شریانی تاثیر کمتری بر بازگشت وریدی نسبت به تغییرات مقاومت وریدی، داشته است که در فرمول نشان داده شده است. میانگین فشار سیستمیک مثل فشار شریانی میانگین نیست. میانگین فشار سیستمیک فشار در وریدهای کوچک و وریدچه ها است.
TABLE 3: Factors That Affect Myocardia Contractility
|
Decreased |
Increased |
|
Catecholamine depletion and receptor malfunction |
Catecholamines |
| a and B blockers |
hotropic drugs |
|
Calcium channel blockers |
|
| Decreased preload |
Increased preload |
|
Overstretching of myocardium |
Decreased afterload |
| Severe inflammation and ischemia |
|
ادامه مطلب را با دانلود فایل پیوستی مشاهده کنید.
ورود یا ثبـــت نــــام + فعال کردن اکانت VIP
مزایای اشتراک ویژه : دسترسی به آرشیو هزاران مقالات تخصصی، درخواست مقالات فارسی و انگلیسی، مشاوره رایگان، تخفیف ویژه محصولات سایت و ...
حتما بخوانید:
⇐ تغذیه بیماران دارای عمل جراحی
⇐ آب، الکترولیت و تعادل های اسید باز بیماران جراحی
⇐ ارزیابی قبل و بعد از عمل و مدیریت بیماران جراحی شده
⇐ خونریزی های جراحی: مشکلات خونریزی، انعقاد خون، پیوند عضو در بیماران جراحی شده


دیدگاه خود را ثبت کنید
تمایل دارید در گفتگوها شرکت کنید؟در گفتگو ها شرکت کنید.